Представления о фазовом
переходе расплав – твёрдое тело при стеклообразовании, модель стеклообразного
состояния и некоторые её приложения
Теория строения стекла
Анатолий
Иванович Болутенко
E-mail: bolutenko@mail.ru Физика стекла Главная
Содержание
1. РАЗВИТИЕ И
ЗНАЧЕНИЕ СТЕКЛОДЕЛИЯ
2.2.
Состояние вопроса по развитию теории
2.3.
Сложности в развитии теории стеклообразного состояния
2.4.
Требования к теории
2.5.
Необходимость развития теории
3. СОВРЕМЕННЫЕ
ВЗГЛЯДЫ НА СТЕКЛООБРАЗНОЕ СОСТОЯНИЕ
3.1.
Роль переохлаждения расплава для получения стёкол
3.2.
Метастабильное состояние стекла
3.3.
Стекло – жидкость
3.4.
Жидкостная концепция – основа теории стеклообразного состояния
3.5.
Выводы
4. НОВЫЙ ПОДХОД
К ПОСТРОЕНИЮ ГИПОТЕЗЫ СТЕКЛООБРАЗНОГО СОСТОЯНИЯ
4.1.
О неприменимости критерия переохлаждения
4.2.
Стекло – стабильное состояние
4.4.
Критика жидкостной концепции
4.5.
Реальные и идеальные стёкла
4.6.
Выводы
5. МОДЕЛЬ
СТЕКЛООБРАЗНОГО СОСТОЯНИЯ И СТОРЕНИЕ СТЕКЛА
5.1.
Стеклообразование
5.2.
Характерные признаки стеклообразного состояния
5.2.1.
Причины формирования стеклообразной структуры
5.2.2.
Упорядоченность стёкол
5.3.
Процесс нагревания стёкол
5.4.
Об агрегатном состоянии стекла
5.6.
Некоторые факты, подтверждающие модель
5.7.
Выводы
6. НЕКОТОРЫЕ
ПРИЛОЖЕНИЯ МОДЕЛИ СТЕКЛООБРАЗНОГО СОСТОЯНИЯ
6.1.
Прочность стекла
6.2.
Закалка
6.3.
Вязкость
6.5.
Развитие приложений модели
7. ОБЩИЕ ВЫВОДЫ
А1 1. РАЗВИТИЕ
И ЗНАЧЕНИЕ СТЕКЛОДЕЛИЯ
Стекло принадлежит к одному из древнейших
предметов материальной культуры, созданной человеком. Время появления первых
простейших изделий из стекла относится к далёкому прошлому. Первые образцы
стеклянных изделий, надёжно и уверенно датируемые археологами, относятся к 35
веку до н.э. Вероятно, с этого времени начинается применение стекла человеком
как материала. Есть достаточные основания утверждать, что открытие стекла надо
связывать с началом плавки металлов и получением металлургических шлаков.
Большого расцвета производство стекла
достигло в Египте 1500 лет до н.э. В Италию стеклоделие проникло из Египта в 1
веке до н.э., а из Рима распространилось по всей Европе, в т.ч. и на Руси. В 10
– 11 веках в Киеве было развито производство стеклянных и эмалевых украшений.
Первый стекольный завод построен в России близ Воскресенска в 1635 году.
Стекло является одним из важнейших
искусственных материалов, прочно вошедших в быт, культуру и технику людей всего
мира. Ещё сто лет назад области применения стекла были довольно ограничены.
Фактически из него изготовляли только посуду, оконное стекло, ювелирные изделия
и оптическое стекло. Однако, к концу 19 века стекло уже играло большую роль в
техническом и культурном прогрессе человечества.
Трудно переоценить роль стекла в настоящее
время в качестве электроизоляционного, электровакуумного, стекловолокна, в т.ч.
для световодов, подложек для микроэлектроники, строительного стекла,
химического и новых особо прочных и термостойких материалов на основе стекла –
ситаллов и других видов изделий.
А2 2. РАЗВИТИЕ
НАУКИ О СТЕКЛЕ
Возникновение и развитие представлений о
физико-химической природе стекла связано с историей химической науки в целом.
Первым русским учёным и основоположником научного стеклоделия в России является
М.В.Ломоносов, который с начала организации первой научной химической
лаборатории в 1748 году вёл интенсивную исследовательскую работу по химии и
технологии стекла. Им было впервые осуществлено опробование ряда окислов как
стеклообразующих компонентов.
В конце 18 века – 1798 году М.Клапорт
делает доклад о первых качественных химических анализах нескольких стёкол на
заседании Берлинской академии наук и литературы и закладывает начало
экспериментальных исследований природы силикатных стёкол.
А21
2.1.
Гипотезы строения стекла
В середине 19 века, исходя из
определённого соотношения окислов при стекловарении, была создана гипотеза о
том, что стекло представляет определённое химическое соединение.
Д.И.Менделеев не согласился с
существующими в его время воззрениями на природу стекла и подверг их пересмотру.
В истории развития науки о стекле и его строении Менделеев занимает одно из
важнейших мест. Он в 1856 году защитил диссертацию «Строение кремнезёмистых
соединений», а позже изложил свои взгляды в книге «Стеклянное производство».
Менделеев рассматривал стекло как вещество неопределённого химического состава,
которое не может быть выражено формулой определённого химического соединения и
является неопределённой смесью определённых силикатов.
Г.Тамман определил в 20-х годах 20-го
столетия стекло как «невыкристаллизовавшийся сильно переохлаждённый сплав». В
соответствии с этим основные особенности строения стёкол должны отражать в себе
структуру жидких сред. Тамман изучал свойства жидкостей и сплавов в зависимости
от температуры. Его теоретические воззрения были построены преимущественно на
основе исследования кинетики кристаллизации жидкостей и условий перехода их в
стёкла. Тамман показал, что переохлаждение или же кристаллизация зависят от
скорости образования центров кристаллизации, скорости роста кристаллов и
вязкости охлаждающейся жидкости.
В 1925 году Общество стекольной технологии
устроило дискуссию о строении стекла. Когда был издан сборник, видный
английский исследователь стекла Тернер в обзоре писал: «Я достиг лишь того, что
установил полное несовершенство наших познаний, отсутствие основных данных,
необходимых для того, чтобы предложить какую бы то ни было теорию строения
стекла, даже гипотетическую».
В это же время исследования по отжигу
оптического стекла позволили А.А.Лебедеву в 1921 году построить гипотезу
строения стекла, позже получившую название «кристаллитной». Аномалии свойств
стёкол в температурном интервале 520 – 595 градусов привели к предположению,
что происходят полиморфные превращения α↔δ кварца (около 575
градусов). Это возможно при наличии в стекле микрокристаллитов. По
кристаллитной гипотезе стекло – сложная система, составной частью структуры
которой являются кристаллиты.
На основании сходства механических свойств
стёкол и кристаллов, опираясь на законы кристаллохимии и геометрические
соображения, в 1932 году Захариасен предложил новую гипотезу. По этой гипотезе
структура стекла представляет собой непрерывную структурную сетку, подобно
соответствующей кристаллической сетке, с той существенной разницей, что
кристаллическая сетка является закономерно правильной, в то время как сетка
стеклообразных тел является неправильной. В сложных стёклах щелочные ионы
расположены беспорядочно в дырах кремнекислородных тетраэдров.
В
последующем развивалось много гипотез, вот некоторые из них:
1. Агрегатная гипотеза,
согласно которой при понижении температуры происходят реакции структурирования,
образуются молекулярные агрегаты и комплексы (Ботвинкин).
2. Полимерная концепция, развиваемая
Тарасовым, Бартеневым и др. предполагает, что стеклообразователи – линейные,
разветвлённые или сеточные полимеры.
3. Концепция о
микронеоднородной структуре, развитая Порай-Кошицем, исходя из структурных
данных.
Наиболее популярными гипотезами были
кристаллитная теория Лебедева и неупорядоченной стеклообразной сетки
Захариасена. Все выдвигаемые гипотезы подвержены критике в литературе.
Характерной чертой этих гипотез строения стёкол явилось то, что они были
построены на основе какого-либо одного факта и поэтому отражали одну
какую-нибудь сторону сложного и многогранного вопроса строения стекла. Для
объяснения стеклообразования и физико-химических свойств стёкол гипотезы
никогда не применялись, так как и не претендовали на эту роль.
Создалось такое положение, что ни одна
гипотеза не является предпочтительной. В последние 10 лет * не выдвигалось
новых гипотез стеклообразного состояния.
* По состоянию на 1977 год.
А22
2.2.
Состояние вопроса по развитию теории
На протяжении последних пятидесяти лет
изучение структуры неорганических стёкол и построение общей теории
стеклообразного состояния стало важнейшим направлением в исследовании стёкол.
Несмотря на значительный вклад учёных многих стран мира в исследование свойств
и структуры стеклообразных материалов, уровень знаний в области стеклообразного
состояния значительно отстаёт от соответствующего уровня знаний в области
кристаллических веществ.
Несколькими поколениями учёных предложен
целый ряд теорий, гипотез, предположений. Иногда уже казалось, что для полного
понимания природы стеклообразного состояния надо сделать только шаг, что вопрос
о структуре стекла не так сложен, и можно составить о ней весьма ясное представление.
Однако, предложенные теории и гипотезы не
могли объяснить экспериментальные результаты. Много надежд возлагалось на новые
методы исследования. Многие из них уже устарели, а проблема стеклообразного
состояния всё ещё не решена.
В публикациях по стеклообразному состоянию
и свойствам стёкол предложен целый ряд противоречивых взглядов (не претендующих
на роль гипотез) на структуру стекла и объяснение концентрационных и
температурных зависимостей физико-химических свойств. Это даже не две группы
противоречивых мнений, а целая серия сосуществующих разнообразных
предположений. Такое положение сложилось благодаря тому, что не была
убедительно доказана неправомочность большинства из этих взглядов. Зачастую
экспериментальный материал, приводимый в доказательство правильности
предположения, с успехом может быть использован для подтверждения другого
взгляда. Появлялись новые гипотезы и суждения о структуре стекла, а старые
мирно сосуществовали с ними.
Так как предложенные гипотезы строения
стёкол не объясняли фактов, были попытки сблизить или объединить различные
взгляды и на этой основе создать общую теорию. Этот путь не привёл к успеху.
Накопленные экспериментальные данные на
основе выдвинутых гипотез объяснить сколько-нибудь приемлемо не представляется
возможным. Это породило ряд частных гипотез, созданных на основе исследования
одного из свойств стекла и объясняющих только зависимости этих свойств. Таких
объяснений зависимости отдельных свойств к настоящему времени существует очень
много, причём нет единства мнений в оценке причины явлений. Хотя такие частные
гипотезы зачастую корректно объясняют явление, они, в сущности, вредны в деле
создания общей теории стеклообразного состояния.
За последние десятилетия многие науки о
материалах совершили качественный скачёк в познании предмета своего изучения.
Несмотря на многовековую историю стекла как материала вопрос о его строении всё
ещё относится к нерешённой проблеме.
В науке о стекле в настоящее время
наметилась тенденция бесконфликтности, когда существующие положения хотя и не
объясняют сущности явлений, однако, считаются незыблемыми.
А23
2.3.
Сложности в развитии теории стеклообразного состояния
Стёкла в отличие от кристаллов имеют
неопределённое расположение атомов. Как указывал Я.И.Френкель в «Кинетической
теории жидкостей», даже строгое обоснование структурных нарушений в кристаллах
представляют собой весьма сложную задачу.
Нет точного объяснения, почему атомы в
кристаллах располагаются в том или ином порядке, теория образования
кристаллических соединений носит качественный характер. Ещё более трудную
задачу представляет описание положения атомов в стёклах. Создание общей теории
строения стекла, объясняющей экспериментальные данные и важной для практики,
является труднейшей задачей.
В отличие от кристаллических материалов,
стёкла имеют широкие возможности варьирования состава, их можно получать в
различных отличающихся друг от друга комбинациях. Разнообразие состава стёкол
и, в основном, сложные зависимости хода свойств от состава значительно
осложняют задачу изучения их структуры. Стёкла разного химического состава
имеют различное строение, однако, несомненно, существуют общие закономерности,
присущие всем стёклам.
А24
2.4.
Требования к теории
Основой теории стеклообразного состояния
должны быть не надуманные умозрительные представления, а положения и явления с
глубоким физическим смыслом.
Необходимо, чтобы в гипотезе не только
конечные выводы, но и исходные положения отвечали действительности. Гипотеза
строения стекла не должна противоречить экспериментальным данным структурных
исследований, если эти данные однозначны и вытекают из строгой теории
используемых методов. Если гипотеза правильна, она должна предсказывать новые
факты, способствовать улучшению существующей технологии, указывать ей новые
возможности.
А25
2.5.
Необходимость развития теории
Необычайно бурные темпы развития технического
прогресса во второй половине 20 века потребовали применения новых материалов,
обладающих комплексом специфических свойств. Особое значение в настоящее время
приобретают материалы с неограниченной сырьевой базой, к которым относятся
стёкла.
За
длительное время исследования стёкол накопилась огромная информация, однако,
для науки важны те только факты, а прежде всего их объяснение. Появляются новые
важные экспериментальные работы и возникают интересные и принципиальные идеи,
но вопрос о природе стеклообразного состояния как был глубоко запутан и неясен,
таким остаётся и поныне. Правильно понять и объяснить экспериментальные
результаты по свойствам стёкол можно лишь на основе теории стеклообразного
состояния.
Вопрос о строении стекла – не просто
отвлечённая научная проблема. Ещё совсем недавно стеклоделие мало отличалось от
того, каким было сто лет назад, но в последнее время произошёл большой
качественный скачёк. С поразительной быстротой создаются новые материалы на
основе стекла, в практическом стеклоделии стали применять ряд нетрадиционных
химических элементов. При этом поиск и освоение новых стёкол проводится методом
проб и ошибок. В ряде случаев техническая пригодность изделий из стекла
определяется уже не только микросвойствами, но и внутренним строением. Для
совершенствования технологии и создания стёкол с новыми свойствами требуется
глубокое понимание структуры стекла. Кроме прикладного значения для управления
свойствами стекла развитие теории стеклообразного состояния чрезвычайно важно
для современной физики и химии твёрдого тела. Создание общей теории
стеклообразного состояния является насущной задачей, решение которой необходимо
для дальнейшего развития науки о стекле.
Теория – эффективность науки. Если
какой-либо вопрос уточнён бесповоротно и окончательно, не нужно нести
материальные затраты по дальнейшему бесконечному решению проблемы.
А3 3.
СОВРЕМЕННЫЕ ВЗГЛЯДЫ НА СТЕКЛООБРАЗНОЕ СОСТОЯНИЕ
А31
3.1.
Роль переохлаждения расплава для получения стёкол
Идея Г.Таммана о стекле как
переохлаждённой жидкости была значительным вкладом в науку о стекле.
Представления о стекле как переохлаждённом расплаве по-прежнему не потеряло
своего значения и является ценной физико-химической схемой для понимания
процессов стеклообразования.
Роль переохлаждения в процессе получения
стекла отражена в формулировке стекла, разработанной комиссией по терминологии
при АН СССР в 1939 году. По определению этой комиссии стеклом называются все
аморфные тела, полученные путём переохлаждения расплава независимо от
химического состава и температурной области затвердевания и обладающие в
результате постепенного повышения вязкости механическими свойствами твёрдых
тел; процесс перехода из жидкого состояния в стеклообразное должен быть
обязательно обратимым. В науке положение о стекле как переохлаждённой жидкости
сейчас общепринято. Стекло – переохлаждённая жидкость с ненормально высокой
вязкостью.
Стеклообразное состояние – неравновесное
состояние переохлаждённой жидкости. Хотя, впервые выдвинувший идею
переохлаждения, Тамман считал, что переохлаждённая жидкость не полностью
описывает соотношение между жидким и стеклообразным состоянием, а показывает,
каким образом можно превратить жидкость в стекло.
По А.А.Аппену определение стекла как
переохлаждённой жидкости вытекает из способа получения стекла. Для перевода
кристаллического вещества в стеклообразное необходимо его расплавить и
переохладить. Стекло, полученное на практике, не доходит до равновесия.
Стекло переохлаждается в результате повышения
вязкости. Когда расплав доходит до ликвидуса, он не кристаллизуется, а остаётся
жидкостью. Жидкость, находящаяся ниже температуры ликвидуса, далее опять
охлаждается и снова остаётся жидкостью. Следовательно, стекло – переохлаждённая
жидкость (Мазурин).
Во вновь созданном журнале, выпускаемым в
Институте химии силикатов АН СССР «Физика и химия стекла», ведущими
специалистами в 1975 году подтверждено, что в подавляющем большинстве случаев
стёкла получают переохлаждением расплава. Начиная с тридцатых годов, получили
широкое распространение взгляды Таммана на стекло как переохлаждённую жидкость.
И хоть в настоящее время наши знания о природе стеклообразного состояния и о
строении стекла неизмеримо возросли, это таммановское положение по-прежнему
сохраняет силу, поскольку именно переохлаждение расплава пока практически и
используется для получения стёкол.
А32
3.2.
Метастабильное состояние стекла
Из представления о стекле как
переохлаждённой жидкости естественно вытекает представление об его
метастабильном состоянии.
Хотя есть явно противоречащие факты,
например, как трудность получения кристаллических форм B2O3 из стёкол, на что указывал Уоррен (1971),
представления о метастабильном состоянии стекла широко распространены.
Состояние стекла не является устойчивым.
Стекло обладает повышенным запасом внутренней энергии (Аппен, 1954). В отличие
от кристаллов стёкла представляют собой термодинамически неравновесные системы,
относительная устойчивость которых определяется затруднённостью процессов
перестройки структуры из-за весьма сильного взаимодействия между частицами
(Михайлов, 1955)
Переход стекла из жидкого в твёрдое
состояние есть переход из стабильного в одно из нестабильных состояний
(Даувальтер, 1958). Почти все известные стёкла метастабильны при комнатной
температуре, поскольку кристаллическое состояние более устойчиво (Стуки, 1959)
В отличие от кристаллов и жидкостей стёкла
не находятся в термодинамически равновесном состоянии. Поэтому в реальных
стёклах и при температурах ниже температуры стеклования происходит очень
медленная перегруппировка молекул, приводящая к изменению структуры каркаса в
направлении, отвечающем более равновесному состоянию (Шишкин, 1960).
В стекловидном состоянии энтальпия системы
выше, чем у кристалла и оно в термодинамическом отношении нестабильно (Бонетти,
1963). Застывший стекловидный расплав представляет собой метастабильное
состояние. Стабильное состояние, характеризуемое наименьшим запасом энергии,
достигается путём кристаллизации (Фогель, 1965). Вследствие беспорядочной сетки
внутренняя энергия текла больше, чем у соответствующего кристалла (Роусон,
1070).
А33
3.3.
Стекло – жидкость
Представление о стекле как переохлаждённой
жидкости одновременно приписывают ему свойства жидкости. Многие авторы при этом
подчёркивают, что стекло – жидкость. Кристаллизация стёкол считается переходом
из стекловидной фазы в твёрдую (Кузнецов, 1959). Вязкость жидкости при
отвердевании стеклообразующего тела ориентировочно оценивается в 1017
пуаз (Аппен, 1970).
Охлаждение жидкости до полного
затвердевания приводит к замораживанию структуры жидкости. Стекло подобно
твёрдому телу (Чарльз, 1970) Стеклообразное и жидкое состояния близки. Однако
время, необходимое для изменения решётки под действием внешних сил для жидкости
мало, а для стёкол велико. В этом отношении стекло ведёт себя как твёрдое тело
(Балашов, 1973).
А34
3.4.
Жидкостная концепция – основа теории стеклообразного состояния
Установление природы и закономерностей
стеклообразного состояния является необычайно сложной задачей, поэтому пытаются
находить аналоги, служащие моделями стекла. В этой связи широкое
распространение получила жидкостная концепция, по которой структура стекла
приравнивается к структуре жидкости. Впервые на чрезвычайно близкое сходство
между стеклообразным и жидким состоянием указал Тамман (1935).
Развитие кристаллитной гипотезы стекла
совпало по времени с квазикристаллическими представлениями о структуре
жидкостей. Это способствовало широкому применению и укреплению жидкостной
концепции при описании строения стёкол. При рассмотрении стекла как
переохлаждённой жидкости структурные особенности жидкого состояния переносились
на структуру стёкол. Идентичность структуры жидких сред и стекла обосновывалась
на основании подобия такого их свойства, как изотропия (Евстропьев, 1955).
Строение стекла считается тесно связанным
со строением жидкости исходя из того, что кривые рассеяния рентгеновских лучей
стёклами и жидкостями сходны (Бартенев, 1960). Ввиду отсутствия дальнего
порядка в структуре стекла и жидкости можно ожидать сходства между их
структурами (Роусон, 1970).
А.Бейзер в книге «Основные представления
современной физики» 1973) указывает, что аналогия между аморфным твёрдым телом
и жидкостью заслуживает внимания, так как она позволяет лучше понять свойства
обоих состояний вещества. Таким образом, подход к рассмотрению стеклообразного
состояния аналогично жидкому сохранился на протяжении длительного периода.
В ряде работ стеклу приписывают строение
того расплава, из которого оно получено. При охлаждении расплава стёкол частицы
не успевают перестроиться в правильную решётку, сохраняется их неупорядоченное
расположение, свойственное жидкому состоянию (Мюллер, 1964).
Применение жидкостной концепции к описанию
структуры стекла привело к взгляду на стеклообразное состояние как жидкое,
отличающееся от нормального жидкого состояния лишь большей величиной вязкости
(Макмиллан, 1967).
А35
3.5.
Выводы
1. Стекло можно получить только
переохлаждением расплава.
2. Стекло представляет собой отвердевшую
при температуре стеклования жидкость.
3. Стекло – переохлаждённая жидкость.
4. Стеклообразное состояние –
метастабильно, оно обладает повышенным запасом внутренней энергии.
5. Стеклообразное и жидкое состояния
близки, однако, стекло ведёт себя как твёрдое тело.
6.
Стекло отличается от твёрдых тел неупорядоченностью структуры.
7. Стекло относится к аморфным телам.
8. Характерным признаком стеклообразного
состояния является отсутствие симметрии и дальнего порядка.
9. Структура стёкол обладает ближним
порядком.
10. Только посредством жидкости, через её
структуру, можно понять строение стёкол.
А4 4. НОВЫЙ
ПОДХОД К ПОСТРОЕНИЮ ГИПОТЕЗЫ СТЕКЛООБРАЗНОГО СОСТОЯНИЯ
В науке в последнее десятилетие распространилось
мнение, что общей теории стеклообразного состояния не существует и её
невозможно создать. Такой вывод явился естественным результатом неплодотворных
усилий в этом направлении. Поэтому построение теории стеклообразного состояния
требует принципиально нового подхода, который не является иной интерпретацией в
рамках существующих критериев, а в корне изменяет эти критерии и взгляды.
Потребность синтеза новых стёкол для
различных областей техники выдвигает необходимость прогнозирования их свойств.
В связи с этим проблема строения стекла имеет не только теоретический интерес,
а приобретает большое практическое значение. Определение структуры стекла
заключается в установлении характера расположения его отдельных элементов и
типа образуемых между ними связей. Знание структуры в свою очередь
предопределяет объяснение процесса фазового перехода расплав – твёрдое тело при
стеклообразовании и физико-химических свойств различных стёкол.
В связи со сложностью стекла как системы с
неопределённым расположением атомов следует стремиться понять не частные
элементы структуры, а общие принципы и закономерности стеклообразного
состояния.
К настоящему времени накопилось множество
экспериментальных фактов, дальнейшая работа в этом направлении в большинстве
случаев не даёт новой информации. Едва ли следует ожидать получения
экспериментальных данных, которые внесут коренной перелом в представления о
стеклообразном состоянии и послужат основой для построения теории. Необходимо
ориентироваться на имеющийся материал, полученный различными методами, который
требует осмысления, обобщения, теоретического обсуждения и должен явиться
основой для построения теории стеклообразного состояния.
На основе анализа и обобщения большого количества
публикаций по гипотезам строения стекла, температурным и концентрационным
зависимостям физико-химических свойств нами предложен новый подход к решению
вопроса о природе стекла.
А41 4.1. О
неприменимости критерия переохлаждения
Прежде всего, следует сказать в отношении
неорганических стёкол, что хотя переохлаждение считается неотъемлемым от
стеклообразного состояния, но это не факт, доказанный экспериментом, а всего
лишь гипотеза. Независимо от масштабов признания любой гипотезы, пока она не
превратилась в теорию, имеет право на существование и любая другая гипотеза.
То, что при охлаждении расплавов
образуются стёкла, а не кристаллы, ещё недостаточный факт для утверждения о
переохлаждении. Таммановские постулаты о переохлаждении в связи с отсутствием
других объяснений стеклообразования были приняты, как аксиома, но в то же время
они легли тяжёлым бременем на сознание людей и препятствуют развитию теории
стеклообразного состояния.
В настоящее время переохлаждение считается
путём, процессом получения стекла. Однако, известно, что понижение температуры
веществ в любом агрегатном состоянии соответствует процессу охлаждения. Поэтому
следует сделать принципиальное замечание, что переохлаждение – не процесс, а
состояние. Система может перейти в это состояние только в результате
охлаждения. Получать стекло переохлаждением или использовать переохлаждение для
этой цели не представляется возможным.
Кроме того, известно, что переохлаждение
является довольно редким случаем и система легко выводится из этого состояния.
Для стёкол же абсолютно всех составов переохлаждение считается основным путём
их получения, при этом переохлаждённое состояние очень устойчиво.
Неоправданной неточностью является
отождествление скорости охлаждения с переохлаждением. Пытаются в гипотезах
путём очень быстрого охлаждения зафиксировать структуру жидкости. Наивно
полагать, что скорость охлаждения будет выше скорости электронных и ионных
процессов перестройки структуры вещества.
Наши представления об отсутствии
какой-либо роли переохлаждения для образования стекла из расплавов развивались
как одно целое с моделью стеклообразного состояния и являются её неотъемлемой
частью.
Следует заметить, что в реальных стёклах в
некоторых случаях возможно переохлаждение относительно отдельных микроучастков
структуры. Но это лишь вторичное переохлаждение, когда ряд атомов не могут
занять свои места в связи с тем, что уже образовалась основная структурная
сетка стекла.
Принцип о стекле как не переохлаждённой
жидкости используется для построения модели процесса фазового перехода
расплавов в твёрдые тела. Он диаметрально противоположен существующему
представлению. Из этого основного принципа как следствие вытекает
представление, что стекло – стабильное твёрдое тело.
А42
4.2.
Стекло – стабильное состояние
Стеклообразное состояние – это состояние
стабильное, а не метастабильное. Если бы стекло было метастабильным,
расстекловывание должно было бы проходить самопроизвольно даже при низких
температурах. Однако, этого не происходит. То, что некоторая часть стекла в
процессе термообработки может перейти в кристаллическую фазу, ещё не говорит о
том, что эта система метастабильна, так как на такой переход надо затратить
внешнюю энергию.
Известно, что метастабильное состояние
является весьма чувствительным к внешним воздействиям. То, что удаётся путём
переохлаждения жидкости получить метастабильное состояние, которое невозможно
перевести в стабильное, говорит о стабильности так называемого «метастабильного
состояния».
Стеклообразное состояние – не
метастабильное, а более стабильное, чем соответствующее данному составу
кристаллическое (ситаллы). В литературе указывается, что самым стабильным состоянием
SiO2 является
кристаллический кварц. Но это не так. Стабильным состоянием при данном давлении
и температуре является то, в которое система возвращается вплоть до
расплавления. При нагревании кристаллического кварца он необратимо переходит в
другие модификации, и затем в кварцевое стекло. Следовательно, стабильным
состоянием SiO2 при нормальном атмосферном давлении является
кварцевое стекло (стекловидное состояние), а все остальные модификации кварца
менее стабильны в ряду: кварцевое стекло – тридимит – кристобалит – кварц.
На стабильность состояния должен указывать
не переход в кристаллическое вещество, а возвращение расплава в то структурное
состояние, которое было до его плавления.
А43
4.3.
Стекло – твёрдое тело
Если в отношении переохлаждения и
вытекающей из него метастабильности стеклообразного состояния имеется в
настоящее время полное единство взглядов, то относительно того, что такое стекло
– твёрдое или жидкое тело, мнения разделились. Взгляды на стекло как
переохлаждённую жидкость рассмотрены выше. Некоторые исследователи
стеклообразного состояния полагают, что стекло – твёрдое тело, получаемое
переохлаждением жидкости.
Ещё Тамман (1935) указывал, что в
стеклообразном состоянии находятся твёрдые некристаллизующиеся вещества. К
твёрдому состоянию стекло относили Мюллер (1965), Куколев (1966).
Под твёрдым телом обычно подразумевается
вещество, которое обладает некоторой жёсткостью по отношению к сдвигу. Такое
качество стёкол известно всем из практики. По твёрдости стёкла занимают
промежуточное положение между железом и закалённой сталью и являются
значительно твёрже многих традиционно твёрдых кристаллических тел – минералов.
Представления о стекле как о жидкости, пусть
даже переохлаждённой, должны приводить к ползучести стёкол под нагрузкой. С
другой стороны известно, что стёкла являются упругими и хрупкими телами. Эти
факты явно не согласуются с утверждениями о стекле как о переохлаждённой
жидкости.
Наши представления о стекле как о не
переохлаждённой жидкости приводят к пониманию стекла как твёрдого тела.
А44
4.4.
Критика жидкостной концепции
Общий характер кривых рассеяния рентгеновских
лучей и изотропия в стёклах и жидкостях не является достаточным условием для
суждения об идентичности их структуры. Выбор жидкости в качестве модели стекла
недостаточно обоснован и был возможен в связи с общностью взглядов гипотез
строения стекла и жидкости как квазикристаллических. Жидкостная концепция
строения стекла носит чисто постулативный характер и недостаточно убедительно
подтверждена экспериментально. Стремление представить структуру стекла
аналогично структуре жидкости требует знания структуры жидкости. В основу
кинетической теории жидкости Я.И.Френкелем положено сближение жидкого состояния
с твёрдым кристаллическим.
Несмотря на то, что созданы теоретические
основы строения жидкостей, нельзя считать окончательно решённым вопрос об их
структуре. В действительности структура жидкости значительно сложнее, чем
структура соответствующего ей твёрдого тела. Это происходит за счёт перехода
части атомов при нагревании в возбуждённое состояние, взаимодействие их с
остальными атомами представляет весьма сложную картину.
В исследовании стеклообразного состояния
сделана ориентация на жидкостную концепцию строения стёкол. Задача расшифровки
структуры самой жидкости оказалась настолько сложной, что моделирование стекла
посредством жидкости привело к усложнению решения вопроса.
Уэрт, Томсон (1969) указывают, что в
жидкостях геометрия расположения атомов недостаточно известна. Прямое
исследование структуры жидкостей является невыполнимой для эксперимента задачей
(Китайгородский, 1969). В связи с тем, что строение жидкости неизвестно,
попытка использования жидкого состояния в качестве модели стеклообразного
состояния неправомочна. Развитие представлений о стеклообразном состоянии из
общего строения жидкости нереально. Считать, что расплав стёкол отражает их
структуру в твёрдом состоянии можно лишь в той мере, в какой это относится к
кристаллическим веществам. Конечно, твёрдое тело имеет непосредственную
генетическую связь с расплавом, из которого оно образовалось. Но именно
благодаря различиям в структуре, возникающим с ростом температуры, и происходит
плавление. Жидкость не может быть использована в качестве модели твёрдого тела
в стеклообразном состоянии. Перспективнее в качестве модели стеклообразного
состояния использовать деформированное кристаллическое твёрдое тело.
А45
4.5.
Реальные и идеальные стёкла
Теоретически можно представить стекло,
которое являет собой повторяющуюся однородную стеклообразную сетку, имеющую
строение в зависимости от химического состава. Однако, незнание точного
соотношения компонентов, их загрязнённости, зависимости структуры стекла от
технологических режимов приводят к появлению неоднородностей в стекле при варке
и выработке.
Естественно, что реальные стёкла далеки от
идеальной стеклообразной структуры. В получении реальных стёкол некоторую роль
может иметь вторичное переохлаждение отдельных микроучастков структуры. Всё
стёкла имеют в своей структуре ликвационные расслоения или кристаллы.
Можно провести следующую классификацию
стёкол:
1.
стекло
2.
стекло – стекло
3.
стекло – стекло –
стекло
4.
стекло – кристалл
– кристалл
5.
стекло – стекло –
кристалл
6.
стекло – стекло –
кристалл и так далее.
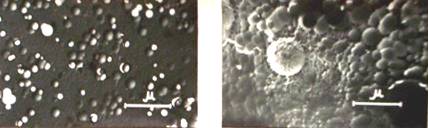
Таким образом, реальные стёкла можно
рассматривать как композиционные материалы, состоящие из собственно стекла с
имеющимися в нём кристаллами различных составов и ликвационными областями,
образованными стёклами иных составов (Рис.1).

1. WO3 – 40, P2O5
– 30, 2. P2O5
– 60, BaO – 40
BaO –
20, TiO2 – 10

3. WO3 – 10, P2O5
– 40, 4. WO3 – 30,
P2O5 – 40,
BaO –
40, TiO2 – 10
BaO – 20, TiO2 – 10
5. WO3 – 40, P2O5
– 20, 6. WO3 –
30, P2O5 – 20,
BaO –
10, TiO2 – 30
BaO – 20, TiO2 – 10
Рис.1
Микроструктура реальных стёкол. Составы приведены в молярных процентах.
В связи с тем, что в природе не существует
и не может существовать идеальных стёкол, и понятие «идеального стекла»
является таким же условным, как «идеального газа», необходимо при исследовании
стёкол учитывать это обстоятельство. Мы знаем, какую положительную роль сыграло
в науке понятие «идеального газа», поэтому рассмотрение «идеального стекла»
является весьма перспективным.
Построение теории стеклообразного
состояния и развитие представлений о характерных свойствах, присущих
стеклообразному состоянию, формировалось на экспериментальном материале
реальных стёкол. Отсюда вытекают те противоречия и разноречивые доводы, которые
появляются с выходом в свет новых работ. Результаты этих работ в большинстве
случаев являются частными, и поэтому не могут служить материалом для создания
общей теории стеклообразного состояния.
Построение гипотез по стеклообразному
состоянию должно базироваться на понятии «идеального стекла». Реальные стёкла
должны рассматриваться как композиционные материалы, состоящие из различных фаз
– стекловидных и кристаллических.
Свойства, присущие стеклообразному
состоянию, и предлагаемая модель стекла рассмотрены с позиций понятия
«идеальное стекло».
А46
4.6.
Выводы
При построении модели стеклообразного
состояния принимались следующие критерии:
1.
Стекло – не
переохлаждённое состояние.
2.
Стекло –
стабильное состояние.
3.
Стекло – твёрдое тело.
4.
Жидкостная
концепция не применима к описанию стёкол.
5.
В основу модели
стеклообразного состояния положено понятие «идеального стекла».
А5 5. МОДЕЛЬ
СТЕКЛООБРАЗНОГО СОСТОЯНИЯ И СТОРЕНИЕ СТЕКЛА
Какое же положение занимает стекло в
системе всех материалов? Рассмотрим однокомпонентные стёкла SiO2
(кварцевое), B2O3
(боратное), P2O5
(фосфатное).
Любому состоянию вещества должны
соответствовать определённые условия (или наоборот). Такими условиями являются
температура, давление и гравитационное поле. Не говоря уже о гравитационном
поле, в исследовании стёкол не учитывается давление, что приводит к потере
важной информации. А ведь в обычных условиях получить однокомпонентное
фосфатное стекло не удаётся – оно улетучивается. Весьма летучи и
однокомпонентные боратные стёкла.
Каким образом может кристаллический кварц
перейти в кварцевое стекло? Конечно, причиной является не переохлаждение, а
переход в состояние структуры, соответствующей определённым температуре и
давлению. Кварцевое стекло сколько угодно долго может сохранять своё состояние.
При плавлении кварца происходят изменения в структуре, и плотность изменяется с
2,65 г/см3 у кварца до 2,21 г/см3 у кварцевого стекла.
Как раз эти изменения и приводят к стеклообразному состоянию кварца.
А51
5.1.
Стеклообразование
По современным представлениям
стеклообразование происходит при охлаждении высоковязких расплавов в результате
переохлаждения жидкости, при этом стекло имеет неупорядоченную структуру и
является аморфным телом. Главным фактором при получении стекла является
переохлаждение расплава. Если кристаллическое вещество при охлаждении до линии
ликвидуса начинает кристаллизоваться, образуя на диаграмме температура – время
площадку скрытой теплоты кристаллообразования, то вязкие расплавы
переохлаждаются, образуя стёкла (Рис.2,3).
В этой связи возникает ряд вопросов.
Почему стекло имеет структуру жидкости, а не жидкость структуру стекла? По
аналогии, какую же структуру имеет кристалл? Если бы стекло имело структуру
жидкости, оно должно было бы находиться в жидком состоянии, так как структура
отражает те условия, в которых находится тело.
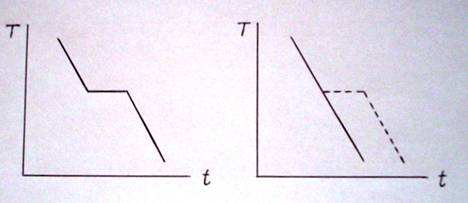
Рис. 2 Фазовый переход
расплава при охлаждении Рис.3
Образование стекла при охлаждении жидкости
и образование кристаллической
структуры
Стекло обычно образуется из высоковязкого
расплава. Вязкость считается фактором, который препятствует росту кристаллов и
приводит к переохлаждению.
По нашим представлениям стекло получается
не в результате высокой вязкости расплава, а расплав имеет высокую вязкость
именно потому, что является стеклом. Из маловязких расплавов нельзя получить
стёкла не из-за низкой вязкости, а потому что это просто не стёкла, а расплавы
кристаллов или смесей кристаллов.
Стекло уже в расплаве стекло. В расплаве
стёкол имеется целый ряд установившихся жёстких химических связей. В расплаве
кристалла все связи разорваны, и изменения температуры выше температуры
ликвидуса изменяет только внутреннюю энергию системы атомов. Изменение же
температуры расплава стекла приводит к значительному изменению вязкости за счёт
разрыва или восстановления химических связей.
Неупорядоченность структуры стёкол приводит
к существованию в стекле непрерывно набора связей по силе и монотонному
изменении свойств. По нашим представлениям в стекле существует дискретный
спектр связей по их силе. При этом, связи не обязательно должны быть
идентичными по структуре, а только по силе связи (в т.ч. и по структуре). Тогда
при охлаждении расплава восстанавливается химические связи определённой силы.
Это восстановление связей аналогично кристаллообразованию при охлаждении
расплава. Поэтому при охлаждении расплава стекла с закреплением связей
выделяется скрытая теплота структурообразования, и с течением времени снижение
температуры становится непропорциональным времени. На диаграмме время –
температура при охлаждении стеклообразного расплава для каждой группы с
одинаковой силой связи имеется своя линия ликвидуса (Рис.4).
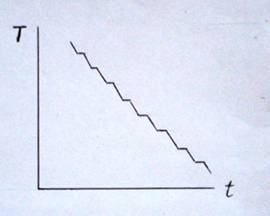
Рис.4
Фазовые переходы стеклообразных расплавов в твёрдое состояние
при охлаждении и структурообразование
стёкол
При этом в каждой группе связей может
быть различное количество. В зависимости от химического состава стеклообразного
расплава в нём может варьироваться периодичность дискретности связей по
группам, и количество связей в каждой группе может быть различным. В случае,
если набор связей имеет постепенный непрерывный переход – дискретность
пропадает. Распределение связей по их силе будет представлять непрерывный ряд.
Этот частный случай соответствует общепринятым представлениям о структуре
стекла.
А52
5.2.
Характерные признаки стеклообразного состояния
А521
5.2.1.
Причины формирования стеклообразной структуры
Стекло – не переохлаждённая жидкость, а
структура, состоящая из такого набора атомов, который не может составить
упорядоченного кристаллического соединения в силу распределения зарядов атомов.
Положение атомов компонентов, входящих в стекло, характеризуется их
электрическими зарядами. Именно электрический заряд атомов расставляет их в
определённом порядке. Все ионы в структуре стекла находятся в узлах равновесия.
Это есть узлы стеклообразной решётки. Располагаться в междоузлиях ионы не
могут, так как для ионов в структуре таковых не существует – где в данный
момент находится ион, там находится и узел.
Любой переход ионов в новое место за счёт
диффузии или при электропроводности ведёт к немедленной реакции структуры,
которая может перейти в напряжённое состояние вплоть до перестройки в зоне её
возмущения. На новом местонахождении каждого иона образуются новые связи.
Стеклообразная структура, таким образом, постоянно находится в динамическом равновесии.
При некоторой температуре в массе вещества
имеется равновесие атомов согласно их заряда, и фактически нельзя сказать, что
данному аниону принадлежит именно этот катион. Любой ион уравновешивает своим
электрическим полем все заряды, координирующие с ним. При этом основная часть
заряда идёт на взаимодействие с первой координирующей сферой, на следующие
сферы воздействие заряда очень резко уменьшается. Одинаковые заряды в различных
катионах неравнозначны. Имеет значение ионный радиус катиона и количество
экранирующих его элементов.
Есть ли в стекле химические соединения? В
нормальных условиях для кристаллических веществ химическое соединение всегда
определённо. Химическое соединение – это возможность взаимного сосуществования атомов,
способных прочно удерживаться друг возле друга. С этой точки зрения в стекле
есть химические соединения, но они неопределённого состава.
Что же удерживает все атомы стекла в
едином блоке? Такой силой является коллективная химическая связь. Силами,
приводящими к монолиту, к единой большой «молекуле» являются силы
неуравновешивания электрического заряда в каждом элементарном объёме стекла.
Это неуравновешивание происходит в связи с асимметрией структуры из-за
соответствующего набора атомов. Различия по силе химической связи в твёрдом
теле как раз и определяют природу стеклообразного состояния.
В связи с невозможностью точного
сбалансирования электрических зарядов ионов в стёклах, как и в кристаллических
телах, имеются несовершенства структуры. Однако, стёкла являются твёрдыми
телами не со случайной, а с постоянной структурой, соответствующей
определённому химическому составу. Получение воспроизводимости
экспериментальных данных по плотности и другим физико-химическим свойствам
указывает на закономерности в образовании структуры стёкол.
Так как стёкла в большинстве случаев
являются техническими продуктами и возможны очень широкие варианты выбора их
химического состава, взаимодействие ионов может приводить к образованию
структур различного типа. Положим, что в стёклах отсутствуют
микронеоднородности и ликвационный распад. В этом случае равновесное состояние
системы определяется её устойчивостью. Степень устойчивости стеклообразной
структуры может быть разная. При определённом наборе ионов устойчивость
стеклообразной структуры будет очень низкой. Это даёт возможность перейти
системе в другое состояние. Чрезвычайно низкую устойчивость системы можно
характеризовать как переохлаждённое состояние. Стеклообразные системы с низкой
степенью устойчивости являются частным случаем современных представлений о
стёклах, как переохлаждённых жидкостях.
А522
5.2.2.
Упорядоченность стёкол
Наличие ликвации и микронеоднородностей в
реальных стёклах свидетельствуют о том, что в каждом конкретном случае
структура стекла является не просто случайностью, а строго определённой. В
случае аморфной, неупорядоченной структуры в стекле не было бы никаких
микронеоднородностей, происходило бы полное взаимное растворение фаз.
Практически можно получать только
неоднородные в микрообластях стёкла, однако, если не рассматривать эти
микрообласти и граничащие с ними участки, структура стекла является однородной.
Стеклообразная структура является также вполне естественной, как и все другие.
В стекле существует статистическая упорядоченность, иначе свойства в различных
областях были бы разными.
Разнообразие различных комплексов в
стёклах очень велико. Исходя из представлений о структуре стекла как о наборе
различных связей, среди которых есть идентичные, можно говорить о наличии в
стеле дальнего порядка. В отличие от дальнего порядка в кристаллах, которые
состоят из подобных элементов ячеек и допускают трансляцию элементарной ячейки
на любое количество узлов решётки, дальний порядок в стёклах можно определять
как приведенный дальний порядок.
Приведенный дальний порядок в стекле
полагает возможность трансляции элементарной ячейки на некоторое расстояние с
одновременным вращением её на некоторый угол. Элементарная ячейка может состоять
из любого количества элементов, элементарных ячеек в стекле множество. При этом
количество элементарных ячеек соответствует числу уровней дискретности при
переходе из расплава в твёрдое стекло.
Упорядоченность стекла характеризуется
тем, что в данных условиях образуется самая стабильная ситуация в расположении
ионов. Из положения о наличии приведенного дальнего порядка в стекле и из
представлений о построении структуры стекла вытекает, что стекло не может иметь
ближнего порядка.
В настоящее время распространено
представление о наличии ближнего порядка и отсутствии дальнего на основании
представлений о стекле как жидкости. Признание наличия ближнего порядка
обязательно должно привести к признанию дальнего путём рассмотрения
последовательного ряда соседних атомов (закон транзитивности). Если A → B, B → C, то A → C и т.д.
Ближний порядок в реальных стёклах может
быть лишь в микронеоднородном стекле в областях неоднородности, которые по
своему строению приближаются к кристаллам.
Итак, по нашим представлениям структура
стёкол не имеет ближнего порядка в расположении атомов, но имеет дальний
приведенный порядок.
Схематически кристаллы,
стёкла по существующим представлениям и по развиваемой модели представлены на
рисунках 5, 6, 7.
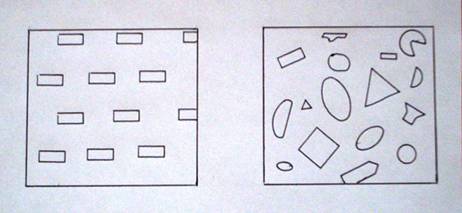
Рис.5
Строение кристаллов Рис.6
Строение стёкол по существующим представлениям
(нет идентичных участков)
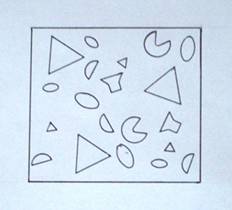
Рис.7
Строение стёкол по предложенной модели (есть одинаковые,
но по разному ориентированные
участки).
Как частный случай возможен
такой химический состав стекла, что схема рис.7 будет идентична схеме рис.6 в
том смысле, что стекло не будет иметь приведенного дальнего порядка, но ближний
порядок вообще не присущ стеклообразному состоянию. Как раз отсутствие ближнего
порядка в стёклах и является главным их отличием от кристаллов в твёрдом
состоянии стекла.
А53
5.3.
Процесс нагревания стёкол
Повышение температуры стекла приводит к
изменению физико-химических свойств, что связано с изменением самой системы.
Отсюда появляется сложность в объяснении экспериментальных данных, и зачастую
возникают необъяснимые явления, называемые аномалиями свойств.
При нагревании или охлаждении
кристаллических веществ изменяется кинетическая энергия ионов, однако, их
расположение относительно друг друга не меняется. Местоположением иона можно
считать среднее положение при его колебаниях. Температура плавления
кристаллических веществ – легко фиксируемая экспериментально температура, при
которой происходит резкий переход в другое энергетическое состояние. Это
происходит потому, что в кристаллических веществах сила связей одинакова. Когда
кинетическая энергия достигает силы химической связи, происходит её разрыв.
Стекло представляет собой иную картину.
При его нагревании начинают увеличивать свою кинетическую энергию все ионы,
однако, благодаря наличию в стекле целого спектра химических связей по их силе,
происходит поэтапный их разрыв. Когда разрываются самые слабые связи, система
немедленно реагирует на этот факт. Разрыв связей немедленно ведёт к изменению
местонахождения остальных ионов – система деформируется для сохранения устойчивости.
Так проявляется изменение структуры в стеклообразной системе при нагревании.
Следовательно, стекло – это упорядоченная
система с переменной структурой, которая при повышении температуры изменяет не
только кинетическую энергию ионов, а также их относительное расположение.
Теоретически вполне возможно, что даже при
комнатной температуре есть связи, для которых эта температура является
достаточной для их разрыва. Такие стёкла будут очень значительно изменять свои
физико-химические свойства при охлаждении.
Выше температуры начала размягчения –
разрыва первых связей с ростом температуры, стекло хотя и представляет твёрдое
тело, но это уже гетерогенная система твёрдое тело – жидкость. По своей
конституции ионы с разорванными связями представляют жидкую фазу в
стеклообразном твёрдом теле. Дальнейший разрыв связей приводит к уменьшению
устойчивости системы и возможности переключения ещё жёстких связей. Тело
становится упруго-вязким. Процесс нагревания далее приводит к разрыву следующих
по силе связей и значительному ослаблению ещё не разорванных. Тело становится
вязким. Величина вязкости зависит от того, насколько полно произошёл процесс
разрыва дискретного спектра связей.
Таким образом, при нагревании стекло
последовательно изменяет механические свойства и проходит следующие стадии
своего состояния: упругое твёрдое тело; упругая гетерогенная система твёрдое
тело – жидкость; упруго-вязкое тело; вязкое тело. Стекло является хорошей
практической моделью для изучения механических свойств твёрдых тел.
Нагревание реальных стёкол в случае их
низкой устойчивости приводит к выделению кристаллов. Однако, есть целый ряд
стёкол, устойчивых к температурным воздействиям – внешний подвод тепла к
системе не изменяет её агрегатное состояние. Таким стеклом является кварцевое
стекло. В ряду кварц – кварцевое стекло – расплав кварц является нестабильным
состоянием, а стекло и расплав – стабильными. Кристаллическое состояние
вещества не всегда является самым стабильным, идеальное стекло всегда стабильно.
А54
5.4.
Об агрегатном состоянии стекла
Итак, стекло – не переохлаждённая
жидкость, а вполне естественная самостоятельная стеклообразная структура,
необходимое объективное состояние вещества, проявляющееся уже в расплавах.
Агрегатное состояние вещества
определяется, прежде всего, внутренним строением. Существуют газообразное,
жидкое и твёрдое агрегатные состояния вещества. По существующим представлениям
твёрдое тело может быть кристаллическим и аморфным. В кристаллических телах
атомы расположены по строго заданным направлениям и на определённых
расстояниях. Основным признаком кристаллов является наличие резко выраженной
температурой точки плавления. Кристаллы имеют дальний порядок.
Слово «аморфный» означает «лишённый
формы». Аморфные тела противопоставляются кристаллам, представителем аморфных
тел считается обычно стекло. Иными словами, твёрдые тела, у которых отсутствует
дальний порядок, называют аморфными. При нагревании аморфные твёрдые тела
постепенно переходят в жидкости.
В 1927 году Парье и Хафменн высказали
мысль о стекле как «четвёртом состоянии материи». В 30-х годах это положение
развивал Бергер.
Стеклообразование происходит при таком
наборе атомов, когда их заряды при температуре плавления и давлении в 1
атмосферу образуют именно стеклообразную структуру. Для однокомпонентных
кварцевых стёкол переход из кристаллического состояния можно считать изоморфным
состоянием кварца – стеклообразным. Для многокомпонентных стёкол стеклообразное
состояние является формой существования материи.
Стекло – это такое сочетание или
искусственная смесь анионов и катионов, которая при расплавлении не может
создать кристаллическую структуру, атомы вынуждены образовывать то соседство, которое
возможно, и образуют наиболее стабильную в естественных земных условиях
стеклообразную структуру, характеризующуюся различными по силе химическими
связями, определяющими природу стеклообразного состояния.
Аморфного состояния с присущими ему неестественными
свойствами бесформенности в природе просто не существует. Любое твёрдое тело с
любой структурой – это единственно возможная ситуация структуры в данных
условиях. Аморфность же предполагает из одного и того же расплава при одних и
тех же условиях получать различные конечные продукты.
Стеклообразное состояние, наряду с
кристаллическим, является формой существования твёрдых тел. При этом
стеклообразное состояние – наиболее общая форма существования твёрдых тел.
Кристаллическое состояние является частным случаем стеклообразного. Это
вытекает из модели стеклообразного состояния в случае, если положим, что
количество дискретных уровней равно 1, т.е. сила всех связей в гипотетическом
твёрдом теле будет одинакова.
Утверждение о стеклообразном состоянии как
наиболее общей форме твёрдых тел соответствует действительности даже по числу
твёрдых тел, находящихся в твёрдом состоянии, и по разнообразию их структуры.
Известно 230 пространственных групп симметрии Фёдорова – возможных способов
построения кристаллической решётки. В настоящее время известно всего лишь около
2000 различных минералов, из которых только 250-300 широко распространены и
имеют практическое значение (Торопов, 1972).
Количество возможных составов стёкол
практически бесконечно велико. Учитывая количество элементов для введения в
состав стекла, количество компонентов в системе и соотношение этих компонентов,
можно говорить о безграничности возможных вариантов существования твёрдых тел в
стеклообразном состоянии. Укажем лишь на тот факт, что М.В.Ломоносов в 1764
году писал: «Здесь больше четырёх тысяч опытов, коих не только рецепты сочинял,
но и материалы по большей части своими руками развешивал и в печь ставил».
Уже к настоящему времени количество
синтезированных стёкол бесконечно велико. В связи с разнообразием состава и
свойств стёкла находят всё новые и новые области технического применения, где
другие материалы просто бессильны. Недаром, предвидя великое будущее стекла,
М.В.Ломоносов в «Оде о пользе стекла» писал:
Не право о стекле те думают,
Шувалов,
Которые стекло чтят ниже
минералов,
Приманчивым лучом блистающих
в глаза:
Не меньше польза в нём, не
меньше в нём краса.
Пою перед тобой в восторге
похвалу
Не камням дорогим, не злату,
а стеклу.
Учитывая бесконечность возможных составов
стекла можно говорить о стеклообразном состоянии как о наиболее общей форме
существования твёрдых тел.
В настоящее время термин «стеклообразное
состояние» широко распространён. Под таким заголовком вышло несколько сборников
Всесоюзных совещаний по строению стекла. Однако, стеклообразное состояние
означало метастабильную переохлаждённую жидкость с аморфной структурой. Термин
«стеклообразное состояние» следует понимать, как и термин «кристаллическое
состояние», как формы существования твёрдого тела. При этом наиболее
распространённым по массе в природе в литосфере Земли является кристаллическое
состояние, а по возможному разнообразию структур – стеклообразное.
Вещества, которые в настоящее время
считаются аморфными, следует отнести к классу полиморфных кристаллических
веществ, в которых существует целый ряд химических связей, различных по силе.
А55
5.5.
Строение реальных стёкол
Стекло благодаря определённому химическому
составу имеет только ему присущее строение. Входящие в состав стекла атомы
строят стеклообразную решётку только на принципах химической связи. Если набор
атомов такой, что по принципу образования системы с наименьшим внутренним
запасом энергии атомы не могут её создать, происходит расслоение структуры.
Внутренними силами, способствующими этому явлению в расплавах, являются
равнодействующие сил взаимодействия атомов, обеспечивающие расстановку с
минимальной потенциальной энергией.
Таким образом, из модели стеклообразного
состояния вытекает представление о микронеоднородности реальных стёкол. При
этом возможны случаи, когда микрогруппировки имеют состав, способный
закристаллизоваться. Образуются микрокристаллы или же эти микрогруппировки
образуют стекло, отличающееся от основной матрицы по химическому составу, т.е.
происходит ликвационный распад.
В реальных стёклах переохлаждение может
иметь некоторую роль. Переохлаждённые участки можно считать дефектами
стеклообразной структуры. Возможно их самопроизвольное расстекловывание или же
кристаллизация при термообработке со скоростью охлаждения меньшей, чем при
получении стекла.
Переохлаждение наиболее вероятно в сложных
стёклах. Так как стеклообразное состояние определяется давлением и
температурой, то в зависимости от скорости охлаждения некоторые микрообласти
расплава могут или переохладиться в стекло, или закристаллизоваться.
Кристаллизация происходит при скоростях охлаждения, соизмеримых со скоростью
диффузии, обеспечивающей доставку материала для образования кристаллической
фазы. Поэтому при большой скорости охлаждения расплавов можно получить стёкла,
которые кристаллизуются при термообработке в связи с неизмеримостью скорости
диффузии и охлаждения. Такие стёкла при термообработке изменяют свою структуру
для обеспечения равновесного состояния.
Мнение о главенствующей роли
переохлаждения, возможно, так широко распространено и общепринято в связи с
тем, что для получения реальных стёкол (особенно не промышленных, а
синтезируемых исследователями), скорость охлаждения имеет решающее значение.
Итак, микронеоднородность является
характерным признаком реальных стёкол, степень неоднородности может в них широко
варьироваться вплоть до полной однородности структуры. В виде неоднородностей в
стёклах присутствуют кристаллы, ликвационные области и их сочетания. Реальные
стёкла в этой связи являются композиционными материалами, что следует иметь в
виду при исследовании их физико-химических свойств.
Исходя из вышесказанного, исследование
зависимости свойство – состав является некорректным, и результаты многих
экспериментальных работ не могут быть признаны достоверными. Следует
исследовать зависимость свойств от микроструктуры с учётом состава микрофаз, а
также композиционного строения стёкол.
А56
5.6.
Некоторые факты, подтверждающие модель
При определении внутреннего трения твёрдых
стёкол методом крутильных колебаний в зависимости от температуры обнаружены
максимумы и минимумы на кривых логарифмических декрементов колебаний (Гуйе,
Васильев, 1914). В дальнейшем эти результаты были подтверждены (Ридер, Риндон,
1960), (Рис.8).
Термическое расширение стеклянных образцов часто
выражается на графиках в виде двух или нескольких пересекающихся кривых
(Турнер, Уинкс, 1930). Обширные работы по изучению инфракрасных спектров
отражения стёкол и кристаллических силикатов проведены Матосси (1937). Он
нашёл, что стёкла и кристаллические силикаты дают сходные спектры, причём,
последние могут быть лучше объяснены, если принять, что в стекле есть маленькие
кристаллики.
Более позднее исследование ИК-спектров
показало, что частоты в спектрах стёкол и кристаллов имеют группировки с
расположением, сходным с расположением атомов в решётке кристаллического
силиката (Смирнова, 1968).
Были получены аномалии при определении
коэффициентов термического расширения. Считали, что скачкообразное изменение
КТР есть результат погрешности измерения. Тщательно поставленные опыты по
определению температурной зависимости линейного расширения показали, то
зависимость совсем не линейна, а имеет ступенчатый характер (Рис.9),
(Богатырёва, 1970).
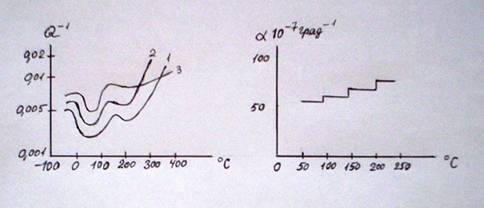
Рис.8 Температурная
зависимость внутреннего трения
Рис. 9 Температурная зависимость линейного
стёкол. 1 – Li2O-3SiO2;
2 – Na2O-3SiO2; 3 – K2O-3SiO2. расширения оптических стёкол
Имеется целый ряд подобных фактов. Когда
эти факты нельзя было объяснить существующими взглядами, они просто относились
в разряд аномалий. Эти и целый ряд других экспериментальных результатов
свидетельствуют о том, что в стекле существует не непрерывны спектр связей по
их силе, а дискретный ряд связей. Структура стекла при нагревании претерпевает
изменения по местонахождению атомов относительно друг друга.
А57
5.7.
Выводы
1.
Стеклообразная
структура образуется уже в расплаве, благодаря чему расплав приобретает высокую
вязкость.
2.
В расплаве стекла
имеется целый ряд установившихся жёстких химических связей, поэтому изменения
температуры приводят к изменению вязкости расплава за счёт разрыва или
восстановления химических связей.
3.
В стёклах существует
дискретный спектр связей по их силе, образующий ряд уровней. В составе стекла
дискретных уровней может быть любое количество, причём, периодичность их и
количество одинаковых связей в одном уровне могут быть разными.
4.
При охлаждении
стеклообразного расплава восстанавливаются химические связи определённого
дискретного уровня – происходит процесс структурообразования.
5.
Во время
структурообразования снижение температуры непропорционально времени – на
диаграмме образуются площадки для каждого уровня прочности химических связей.
6.
Площадки на
диаграмме время – температура представляют линии ликвидуса, для каждой
стеклообразной системы количество линий ликвидуса соответствует числу
дискретных уровней сил связей.
7.
В частном случае,
когда набор связей в системе имеет постепенный непрерывный ряд и дискретность
пропадает, предлагаемая модель стеклообразного состояния описывает современное
общепринятое представление о структуре стекла.
8.
Стекло –
структура, состоящая из такого набора атомов, который не может составить
упорядоченного кристаллического соединения в силу существующего распределения
зарядов.
9.
Ионы в структуре
стекла могут располагаться только в узлах решётки, располагаться в междоузлиях
ионы не могут.
10. Любое перемещение иона в структуре стекла ведёт к
немедленной реакции системы, которая постоянно находится в динамическом
равновесии.
11. Силой, удерживающей стекло в едином блоке, является
коллективная химическая связь и силы неуравновешивания электрического заряда в
каждом элементарном объёме.
12. Различия по силе химической связи в твёрдом теле
определяют природу стеклообразного состояния.
13. Структура стёкол не случайна, а имеет закономерное
построение, о чём свидетельствует воспроизводимость физико-химических свойств.
14. Стабильность стеклообразной системы определяется её
устойчивостью, степень устойчивости структуры может быть разной.
15. Система с очень низкой устойчивостью может
переохладиться и представляет частный случай современных представлений о
стёклах как переохлаждённых жидкостях.
16. Наличие ликвации и микронеоднородностей в структуре
реальных стёкол свидетельствует о закономерности в построении стеклообразных
структур.
17. В стекле существует статистическая упорядоченность, о
чём свидетельствует идентичность свойств в микрообъёмах.
18. Стёкла имеют приведенный дальний порядок,
предполагающий трансляцию элемента структуры на некоторое расстояние с
одновременным её поворотом.
19. Стекло не имеет ближнего порядка, что является его
главным отличием от кристалла.
20. При нагревании стекла разрываются самые слабые связи,
и система немедленно реагирует на это путём изменения местонахождения остальных
ионов – система изменяется, деформируется для сохранения устойчивости.
21. Стекло – это упорядоченная система с переменной
структурой, которая при повышении температуры изменяет не только кинетическую
энергию ионов, а также их относительное расположение.
22. При наличии разорванных структурных связей в стекле
оно представляет гетерогенную систему твёрдое тело – жидкость.
23. Величина вязкости нагретых стёкол зависит от полноты
разрыва дискретного спектра связей.
24. Кристаллическое состояние вещества не всегда является
самым стабильным, стекло всегда стабильно.
25. Однокомпонентные стёкла представляют изоморфное
состояние вещества, для многокомпонентных стёкол стеклообразное состояние
является формой существования материи.
26. Стекло – такое сочетание или искусственная смесь
атомов, вынужденных при расплавлении образовывать ту структуру, которая
соответствует их зарядам и образует наиболее стабильную в естественных земных
условиях стеклообразную структуру, характеризующуюся различными по силе
химическими связями, определяющими природу стеклообразного состояния.
27. Аморфного состояния вещества в природе не существует,
любое твёрдое тело с любой структурой – единственно возможная ситуация
структуры в данных условиях.
28. Стеклообразное и кристаллическое состояния являются
формами существования твёрдых тел.
29. Стеклообразное состояние – наиболее общая форма
существования твёрдых тел, кристаллическое состояние является частным случаем
стеклообразного.
30. Из модели стеклообразного состояния вытекает
представление о микронеоднородности реальных стёкол. Степень неоднородности
структуры может широко варьироваться вплоть до полной её однородности.
31. В связи с наличием микронеоднородностей – кристаллов и
ликвационных областей, реальные стёкла следует рассматривать как композиционные
материалы.
32. Исследование зависимости свойств от состава –
некорректная постановка эксперимента. Следует исследовать свойства в
зависимости от структуры, учитывая композиционное строение стекла.
33. Вещества, которые в настоящее время считаются
аморфными, следует отнести к классу полиморфных кристаллических веществ, в
которых существует целый ряд химических связей, различных по силе.
А6 6. НЕКОТОРЫЕ
ПРИЛОЖЕНИЯ МОДЕЛИ СТЕКЛООБРАЗНОГО СОСТОЯНИЯ
А61
6.1.
Прочность стекла
Среди всех практических свойств твёрдых
тел наиболее важным является прочность. Неизученность структуры стекла и
отсутствие теории стеклообразного состояния приводят к значительным
затруднениям при исследовании механических свойств стёкол.
Много внимания уделялось определению
теоретической прочности стекла. В связи с неопределённостью структуры
теоретическая прочность оценивалась косвенными методами. Теоретическая
прочность стекла по разным оценкам достигает 1500 – 2000 кг/мм2.
Несмотря на огромную теоретическую прочность практическая прочность стёкол мала
и составляет 5 –15 кг/мм2. Задача практической реализации
теоретической прочности стекла является весьма важной и актуальной. Однако, она
до сих пор не решена. Гриффитс (1921) впервые указал, что несоответствие
технической и теоретической прочности происходит из-за наличия в стекле
тончайших трещин, которые находятся во всём объёме образца. Это была первая
теория прочности. Она хорошо объясняет различие теоретической и реальной
прочности. Главный упор в теории Гриффитса делается на наличие в стекле
микротрещин до начала разрушения. Журков (1967) предполагает, что наличие
микротрещин в стекле до начала разрушения необязательно, они могут зарождаться
самопроизвольно.
Электронномикроскопическое исследование
стёкол показало, что трещины Гриффитса в них отсутствуют. В теории Гриффитса не
учитывается структура материала, не учитываются тепловые флуктуации и
молекулярный процесс разрушения. Однако, она ещё достаточно широко используется
для объяснения экспериментальных данных.
Статистическая теория прочности также
предполагает наличие в стёклах дефектов различной степени опасности, и нашла
широкое применение для объяснения прочности от масштабного фактора.
В противоположность чисто механическим
представлениям о разрыве твёрдого тела в последнее десятилетие получила
развитие кинетическая концепция разрушения твёрдых тел (Журков, 1967).
Разрушение твёрдого тела происходит под действием напряжений и теплового
движения атомов. Разрыв связей осуществляется за счёт термических флуктуаций.
Существует очень много вариантов
объяснения прочности и разрушения стёкол. Ведутся работы по получению
высокопрочных стёкол.
Исходя из наших представлений о стекле как
твёрдом теле с дискретным набором химических связей по их силе, вытекает:
1.
Теоретическая
прочность стекла является чисто условным понятием, не имеющим смысла для
стёкол, так как ныне теоретическая прочность трактуется как сумма прочности
всех сил химических связей. В связи с дискретным распределением по прочности
химические связи в стекле разрушаются не одновременно.
2.
Из представлений
о наличии в стекле связей с различной прочностью вытекает, что стекло –
материал малопрочный, и вести работы, направленные на получение стёкол, близким
по прочности к теоретической, нецелесообразно.
3.
Становится ясным
отсутствие трещин Гриффитса в стекле и одновременно низкая его реальная
прочность. Под нагрузкой в стёклах первоначально разрываются самые слабые связи
и образуются микроразрывы, являющиеся началом трещин.
4.
Последовательность
разрыва групп химических связей по их силе даёт представление о процессе
разрушения. После разрыва самых слабых связей нагрузка перераспределяется на
оставшиеся связи. При этом происходит динамический толчок. Хотя визуально
образец сохраняет живое сечение, при уровне напряжений, способных разрушить
самые слабые связи, наступает лавинообразный перенос нагрузки на другие связи,
и, в конце концов, наступает перегрузка, приводящая к мгновенному
взрывоподобному разрушению.
5.
Из положения
отсутствия ближнего порядка в стёклах вытекает невозможность в них пластических
деформаций, выходящих за пределы электронных оболочек атомов. Стекло является
абсолютно упругим телом. Повышенная способность к деформациям возможна лишь при
нагрузках, вызывающих частичное разрушение самых слабых связей, когда остальные
выдерживают напряжение.
6.
Получение стёкол
с повышенной прочностью за счёт химического состава возможно при
однокомпонентных или же многокомпонентных стёклах. В случае однокомпонентных
стёкол в них имеется меньшее количество дискретных уровней прочности, и если
они обладают достаточной прочностью, прочность стекла высокая. В случае
многокомпонентных стёкол, наоборот, спектр уровней становится широким, и не
возникает значительных динамических перегрузок при разрыве очередного уровня.
7.
Модель дискретных
уровней в стекле объясняет температурную и временную зависимость прочности.
8.
Исходя из
стабильности стеклообразного состояния, и невозможности зафиксировать при
быстром охлаждении структуру жидкости, повышенная прочность стеклянного волокна
не может объясняться получением особого поверхностного слоя.
Таким образом, можно объяснить прочность,
упругость, разрушение стёкол, исходя не из специфической гипотезы прочности
стекла, а из общих представлений о стеклообразном состоянии и строении стекла.
А62
6.2.
Закалка
Явление закалки стекла широко
распространено для повышения прочности. Закалка стёкол известна давно.
Первоначально механизм закалки объяснялся следующим образом: в размягчённом
стекле при быстром охлаждении вначале затвердевают наружные слои, в то время
как внутри сохраняется ещё высокая температура. Поверхностные холодные части
стекла препятствуют свободному сокращению его горячих внутренних участков, в
результате чего при дальнейшем охлаждении наружные слои стекла сжимаются, а
внутренние растягиваются.
В дальнейшем в работах Бартенева (1960) был
сделан пересмотр этого объяснения, считалось, что подобное объяснение закалки
не является точным и исчерпывающим, поскольку не вскрывает физических причин
этого явления. По взглядам Бартенева закалка состоит в замораживании в стекле
температурных деформаций и появлением структурного градиента, вызванного
различными скоростями охлаждения участков стекла. Структура в различных
участках стекла будет различной. Менее плотная структура зафиксируется в
наружных слоях, более плотная – во внутренних слоях.
Взгляды, отражающие изменение структуры
стекла при закалке нашли распространение в других публикациях. Изменения
структурного порядка называют структурно-физическим фактором.
Исходя из наших представлений о
стеклообразовании стекло является стабильным твёрдым телом, и любая практически
возможная скорость охлаждения не может привести к фиксированию структуры
жидкости, или же, что то же, температурных деформаций. Охлаждение с любой
скоростью должно проводить к одной и той же структуре. Первоначальное объяснение
сущности закалки справедливо. Структурный градиент в закалённом стекле связан с
внутренними напряжениями, а не с фиксацией температурных деформаций.
А63
6.3.
Вязкость
По гипотезе вязкости стёкол, развиваемой
Мюллером (1955), вязкое течение заключается в трансформировании, переключении
ковалентных связей. Вязкое течение определяется свободной энергией активации,
которая характеризуется прочностью закреплённых единиц в сетке стекла.
Свободная энергия активации меньше энергии валентной связи.
Вместе с тем указывается, что вязкость
является одной из основных физико-химических характеристик стёкол, однако,
отсутствует теоретическая обоснованность зависимости вязкости от температуры
(Карапетьянц, 1958). В зависимости от способа получения кварцевые стёкла могут
значительно отличаться по вязкости, причины таких различий не всегда ясны
(Леко, 1973). Высокая вязкость и зависимость течения кварцевого расплава от
напряжения сдвига позволяет думать, что в расплаве имеются различного размера и
в различном количестве обрывки цепей и кристаллитные образования (Лясин, 1971).
В стекле замедленный процесс переключения
обуславливается природой короткодействующих парноэлектронных связей. Высокая
энергия активации их лежит в основе повышенной вязкости у стеклообразных
расплавов. Этим объясняется характерное для стёкол постепенное размягчение и
медленное снижение вязкости при повышении температуры (Мюллер, 1965). По
современным представлениям механизм вязкого течения силикатного и других стёкол
состоит в трансформации мостиковых кислородных связей (Немилов, 1973).
Объяснение температурного изменения
вязкости стёкол и зависимости её от химического состава просто и естественно
вытекает из предлагаемой модели. Стекло представляет собой продукт с дискретным
набором химических связей с различной периодичностью дискретности и числом
одинаковых связей в каждом уровне. Вязкость стёкол характеризуется количеством
разорванных связей при данной температуре. В каркасе стекла есть связи, разрыв
которых ещё не может привести к вязкому течению. Это самые слабые связи. При
повышении температуры постепенно разрываются всё новые дискретные уровни
химических связей, ослабляются и перестраиваются оставшиеся. При нагревании
стекло представляет гетерогенную систему жидкость – твёрдое тело. После разрыва
всех химических связей расплав стекла представляет собой одну фазу – жидкую.
Разнообразие хода температурных
зависимостей вязкости различных по химическому составу стёкол связана с
индивидуальным набором в каждом стекле дискретных уровней по силе связи.
А64
6.4.
Влияние на другие науки
Выше указывалось, что кварц,
представленный широким классом минералов, является нестабильным. Наиболее
стабильным состоянием кварца является стеклообразное. Это относится не только к
кварцу, а также к базальту. Базальт представляет собой смесь минералов
плагиоклаза и пироксена. Из базальтов получают стекло в промышленном масштабе.
То обстоятельство, что в существующих условиях ряд минералов после расплавления
не выкристаллизовывается повторно, а образует стёкла, является очень важным
фактом. При этом следует обратить внимание на то, что природных стёкол, имеющих
такой же возраст и распространение, как минералы, не существует.
По предлагаемой модели наиболее стабильным
состоянием не обязательно должно быть кристаллическое вещество, им может быть
также стекло.
Если бы образование Земли из
расплавленного состояния происходило в существующих условиях, большую часть
материков покрывали бы массивы стёкол. То, что стёкол вообще в природе нет, а
кора Земли состоит из кристаллических пород, представляет большой интерес.
Кристаллическое вещество земной коры является элементом памяти тех условий, в
которых оно происходило. В этой связи предлагаемая модель может дать
представления об условиях образования Земли. Отсюда может быть пролит свет на
происхождение Земли, и открываются возможности построения гипотез как о самой
Земле и её нынешнем виде, так и о происхождении жизни на Земле.
Намечается новый стык наук – физики
твёрдого тела и геофизики. То, что модель стеклообразного состояния приводит к
постановке таких вопросов, ещё раз показывает важность проблемы стеклообразного
состояния.
А65
6.5.
Развитие приложений модели
Отсутствие приемлемой гипотезы строения
стекла и стеклообразного состояния не позволяет объяснять экспериментальные
данные по многим физико-химическим свойствам стёкол. В связи с этим для объяснения
каждого свойства и явления в стеклообразном состоянии строятся свои гипотезы,
чрезвычайно противоречащие даже для объяснения одного и того же факта.
Предполагается на основе предлагаемой
модели объяснить с единых позиций всё явления в стеклообразном состоянии и
физико-химические свойства стёкол. Это следующие явления и свойства:
стеклообразование, вязкость, ликвация, кристаллизация, микроструктура стёкол,
диффузия, дефекты в структуре, плотность, электрические, тепловые, химические,
механические, оптические и поверхностные свойства.
Объяснение на основе модели
стеклообразования, прочности, вязкости и закалки стёкол приведены выше.
А7 7. ОБЩИЕ
ВЫВОДЫ
1. Существующие гипотезы стеклообразного
состояния не способны объяснить экспериментальных результатов.
2. Предложена модель стеклообразного
состояния, основанная на представлениях о стекле как стабильном твёрдом теле.
Фазовый переход расплав – твёрдое тело осуществляется за счёт структурообразования
при различных температурах, что на диаграмме температура – время выражается
наличием целого ряда линий ликвидуса.
3.Стекло – такое сочетание или
искусственная смесь атомов, образующих закономерно построенную стеклообразную
структуру в соответствии с их зарядами, наиболее стабильную в естественных
земных условиях, характеризующуюся дискретным набором различных по силе
химических связей, определяющих природу стеклообразного состояния, и
представляющее упорядоченную систему, обладающие переменной структурой и
приведенным дальним порядком.
4. Стеклообразное состояние является
наиболее общей формой существования материи в виде твёрдых тел, кристаллическое
состояние – частный случай стеклообразного.
5. Предлагаемая модель объясняет ряд
признаков, физико-химических свойств и явлений в стеклообразном состоянии. На
основе модели предполагается с единых позиций объяснить экспериментальные
данные по исследованию всех физико-химических свойств стёкол.
6. Предлагаемая модель даст возможность с
единых позиций подойти к вопросам объяснения образования Земли. Возможно
создание нового стыка наук – физика твёрдого тела (стеклообразного) и
геофизика.*
22.01.1977 года, г. Львов
Опубликовано 29.10.2011г., через 34 года после написания.
* На основе предложенной
модели стеклообразного состояния разработана гипотеза образования Земли и жизни
на Земле, и 24.02.2007 опубликована на следующих сайтах:
1. http://ab30br.narod.ru Земля и жизнь (поэма, гипотеза сотворения
Земли и жизни)
2. http://ab33ru.narod.ru Образование Земли и сотворение жизни
(изложение поэмы «Земля и жизнь»)